La investigadora española detrás de un nuevo test rápido para detectar el coronavirus
Laura Lechuga, profesora de investigación del CSIC y jefa de grupo en el Instituto Catalán de Nanociencia y Nanotecnología (ICN2), lidera el ambicioso proyecto CoNVaT cuyo objetivo es la fabricación de un test rápido, barato y de alta sensibilidad para diagnosticar el COVID-19 desde el primer día de infección. “No solo dirá si el virus está o no, sino también en qué cantidad. Esto es importante porque da una idea de cómo de avanzada está la infección”, explica. Los nuevos test deberían estar listos en menos de un año, de cara a futuras oleadas de la epidemia.
Galardonada en 2016 con uno de los premios de Física de la Real Sociedad Española de Física y la Fundación BBVA, Laura Lechuga encabeza este proyecto financiado con más de dos millones de euros por la Unión Europea. La investigación es una de las seleccionadas en la convocatoria rápida europea frente al COVID-19, en el marco del Horizonte 2020 y en ella colaboran además la Universidad de Barcelona, la Universidad Aix-Marsella en Francia y el Instituto Nacional de Enfermedades Infecciosas en Italia.
Los test sobre los que están trabajando son biosensores que emplean nanofotónica para detectar proteínas del virus y su material genético. La investigadora es la creadora de este tipo de nanobiosensores y cuenta con gran experiencia en su puesta a punto para diversas patologías usando muestras clínicas. Es por ello que el proyecto ha podido comprometerse a estar listo en menos de un año, plazo que incluye la validación con un elevado número de pacientes.
La principal ventaja que plantea el dispositivo respecto al resto de test existentes es un chip en el que se implementa la interferometría fotónica, una de las técnicas de medición más sensibles de la física. “La técnica es tan sensible que podrá detectar la presencia del virus desde el primer día de la infección”, explica Lechuga. “Y no solo dirá si el virus está o no, sino también en qué cantidad. Esto es importante porque da una idea de cómo de avanzada está la infección”. El sensor se basa en la idea de que cuando un haz de luz se cruza con un objeto, sufre cambios pequeños pero medibles que alertarán de la presencia del virus en la muestra.
Test de bajo coste y que no requieren de personal cualificado
La prueba podrá llevarse a cabo en centros de salud o en puntos de toma de muestras, no necesita de técnicos especializados -algo indispensable con la PCR-, previsiblemente se usarán muestras de saliva y dará resultados en menos de treinta minutos. El dispositivo será del tamaño de una caja de zapatos, pero en su núcleo, donde tiene lugar la medición, todo ocurre a escala nanométrica.

Laura Lechuga en el laboratorio - Instituto Catalán de Nanociencia y Nanotecnología (ICN2)
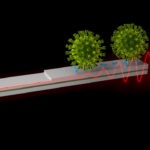
Los investigadores lo denominan como una nanotrampa para proteínas: fijan sobre el chip proteínas diseñadas para atrapar aquellas que se encuentran en la cubierta del virus para hacerlas encajar. En el chip se han grabado además canales de unos nanómetros de grosor por los que pasa la luz, guías que forman un circuito con una única entrada pero que se bifurca, de forma que solo una de las ramas pasa por la trampa de proteínas. Cuando ambos haces de luz se encuentran de nuevo se observa que el que ha interaccionado con las proteínas ha sufrido modificaciones. El análisis de estos cambios delata la presencia y la cantidad del virus.
El dispositivo para detectar material genético del virus se basa en el mismo principio, pero deberá realizarse en el laboratorio. Lechuga explica que su fin será sobre todo confirmar el resultado del primero.
Experiencia en el uso de la nanotecnología
“Una de las razones por las que hemos conseguido el proyecto CoNVaT es que tenemos experiencia con muestras clínicas, que es realmente un mundo completamente distinto al del laboratorio”, explica. Se trata de una tecnología muy sofisticada pero ya validada en la clínica. El Grupo de Biosensores y Aplicaciones Bioanalíticas del ICN2 que dirige Lechuga ha desarrollado, entre otros, nano-biosensores para detectar cáncer de colon precozmente en muestras de sangre, y también para tuberculosis y para casos de sepsis.
“En este tipo de dispositivos la parte biológica es con mucho lo más complejo”, explica. Anclar las proteínas al chip en el ángulo correcto, estabilizarlas para resistir movimiento, mantenerlas en un medio líquido… “son una treintena de pasos”.
El objetivo, al finalizar el proyecto, es que una empresa se ocupe de escalar la tecnología para llevarla al mercado a un precio asequible. “Especialmente en una situación como la actual, trabajamos con la idea de que nuestro trabajo pueda llegar a todos, cuanto antes”, concluye.